聆听跨学科专家小组讨论,包括Samra Turajlic(弗朗西斯·克里克研究所)、Rong Fan(耶鲁大学)和Christina Leslie(纪念斯隆-凯特琳癌症中心),分享他们在多组学研究中的进展与挑战。
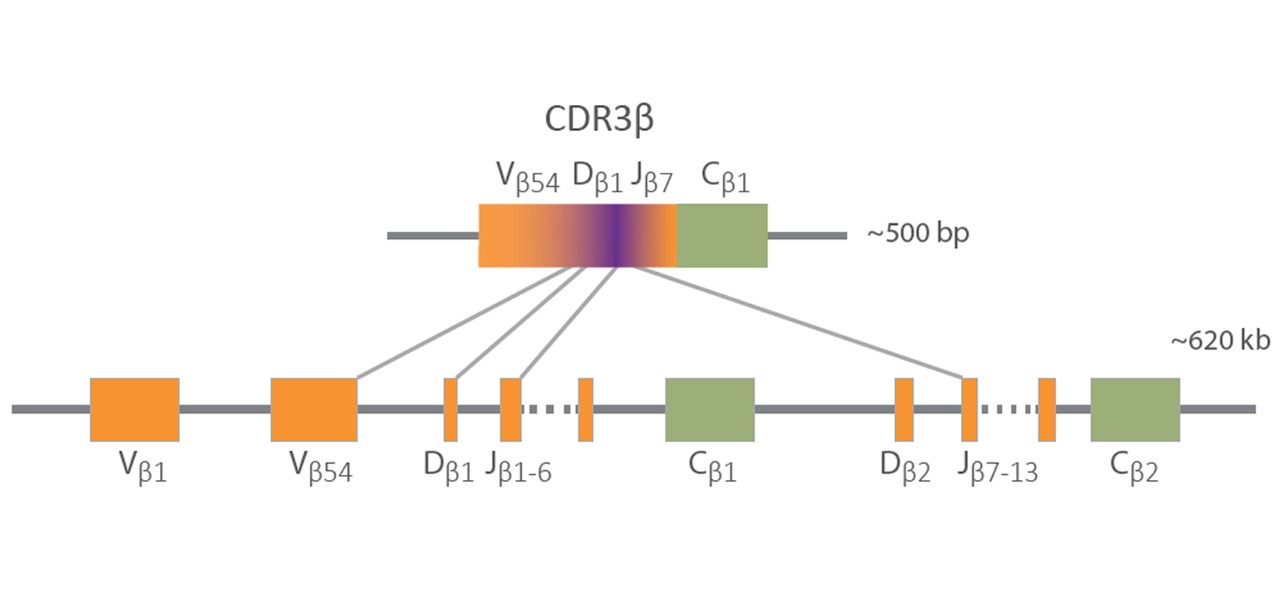
免疫组库测序(IR-Seq)利用新一代测序(NGS)技术对B细胞受体(BCR)和T细胞受体(TCR)的多样性进行分析。¹ IR-Seq使研究人员能够表征组库多样性和克隆性,并研究与血液系统恶性肿瘤、自身免疫性疾病及其他疾病相关的受体序列。² IR-Seq提供所需的高通量和灵敏度,以高分辨率分析BCR和TCR,从而深入了解健康和疾病状态下的适应性免疫。
BCR和TCR序列的免疫组库在应对感染、自身免疫性疾病和癌症时是动态变化的。在免疫应答过程中,循环抗原受体的组库会从多样化群体转变为以扩增的抗原特异性克隆为主的群体。因此,理解免疫组库的组成对于深化我们对免疫介导疾病的认识以及指导治疗开发至关重要。³